利用生物可降解聚合物治疗骨相关疾病已成为生物医学领域的研究热点。最近材料技术的进步扩大了适用于骨科植入物的材料范围。三维(3D)打印技术在医疗保健领域已经变得普遍,虽然器官打印仍处于早期阶段,面临道德和技术障碍,但3D打印能够创建支持和可控的3D结构。该技术在组织工程和再生医学等领域显示出前景,细胞和生物打印以及打印材料的新创新扩大了其可能性。在临床环境中,生物可降解金属的3D打印主要用于骨科和口腔医学。3d打印的患者专用截骨器械、骨科植入物和牙科植入物已被美国FDA批准用于临床。金属通常用于为硬组织提供支撑并防止并发症。目前,临床上使用的种植体有70-80%由铌、钽、镍钛诺、钛合金、钴铬合金和不锈钢制成。然而,人们对诸如镁、钙、锌和铁等可生物降解金属的兴趣越来越大,最近有了许多发现。3D打印具有制造成本低、几何形状复杂、制造周期短等优点,在学术界和工业界得到了广泛的应用。具有可控结构的金属3D打印代表了开发生物医学应用金属植入物的尖端技术。本文综述了3D打印骨科中使用的现有生物材料以及生物可降解金属及其在开发金属医疗植入物和设备中的应用。讨论了该技术面临的挑战和未来的发展方向。
目前,65岁及以上的人口比例接近全球人口的10%,预计到2050年这一数字将增加两倍[1]。由于衰老的影响,这些老年人更容易出现健康问题,包括组织丢失和骨折。解决这些并发症通常需要使用固定、置换或重建手术。由于硬组织的机械要求,金属通常用于这些手术,促进患者活动并防止进一步的并发症[2,3]。骨畸形、骨不连或骨不连骨折、大量骨质流失、肿瘤和影响深远的痛苦损伤等疾病构成了重大的临床挑战,因为传统的外科手术治疗这些疾病的效果有限[4,5]。为了解决这些局限性,引入了骨组织工程(bone tissue engineering, BTE)的概念[6,7]。BTE中一个很有前景的技术是制造三维(3D)合成结构,这些结构可以根据受体的特定需求定制,并且可以容纳细胞和蛋白质的整合[7]。
目前,临床使用的种植体中约有70-80%由铌、钽、镍钛诺、钛合金、钴铬合金和不锈钢组成[8,9,10]。近年来,人们越来越重视对生物可降解金属的研究,包括钙、锌、铁和镁。值得注意的是,在过去几年中出现了一些值得注意的发现[11,12,13,14,15]。当这些金属用作临时种植材料时,它们能够最大限度地减少与长期种植材料相关的不良影响。这可以避免二次手术,从而加快组织再生的过程,并尽量减少进一步的创伤。一个值得注意的例子是镁基生物材料的使用,由于其低细胞毒性,与骨组织对齐的适当弹性模量以及有利的骨形成潜力而引起了极大的兴趣[16]。
3D打印是一种将光、计算机、电力、数字控制、机械和新材料等不同元素结合在一起的制造技术,使不同行业的制造革命成为可能[17,18]。近年来,3D打印越来越多地应用于生物医学领域,使人体组织修复成为可能[19]。它的应用扩展到骨科以及牙科种植体、心血管系统和生物人工肝脏[20]。此外,3D打印已被用于医疗电子和微流体设备的开发。
由于金属种植体与骨之间的机械不匹配,存在应力屏蔽的风险,可能导致骨吸收和种植体失败。因此,开发仿生装置需要新的技术。传统的粉末和冶金铸造方法不能创造复杂的内部结构和复杂的外部形状。但随着3D打印的出现,现在可以生产具有调节模量和几乎类似于天然骨的孔隙度的可生物降解金属植入物[21]。这减少了应力屏蔽问题。此外,3D打印具有成本低、可重复性高、制造阶段短、可实现金属植入物的装配线生产力等优点。它还与计算机辅助设计(CAD)相连接,可以非常灵活地定制模型。为了匹配特定的组织缺陷,该技术以前所未有的方式实现了定制治疗[22]。为了设计与天然骨的功能和结构特征密切相关的植入物,在这个方向上已经进行了很多努力。
3D打印技术的快速发展已经产生了新的打印方法,克服了激光和电子束打印的缺点。目前,3d打印生物金属主要用于制造组织修复、骨科、牙科以及手术工具的植入物。液态金属和3d打印生物可降解金属的发展最终将扩展到其他生物金属应用,例如生物可降解和/或植入式金属生物电子设备。生物金属的用途,由传统3D打印技术创建的可生物降解金属,以及开发3D打印技术产生的新含义都在本文中讨论。
从数字模型制作实际产品被称为三维(3D)打印[23]。计算机辅助设计(CAD)软件可以与3D建模软件、医学扫描方法或3D扫描仪相结合,生成虚拟3D设计文件。然后使用CAD数据创建几个2D横截面层。然后,无需中间成型阶段,3D打印机根据预设的2D模式创建3D结构[24]。3D打印具有设计自由、自动化、快速生产、可忽略剩余生成、定制化和准确性等优点[25]。3D打印物体的制作过程包括三个关键步骤,即数据采集、图像处理和物体的3D打印(见图1)[24]。
图1
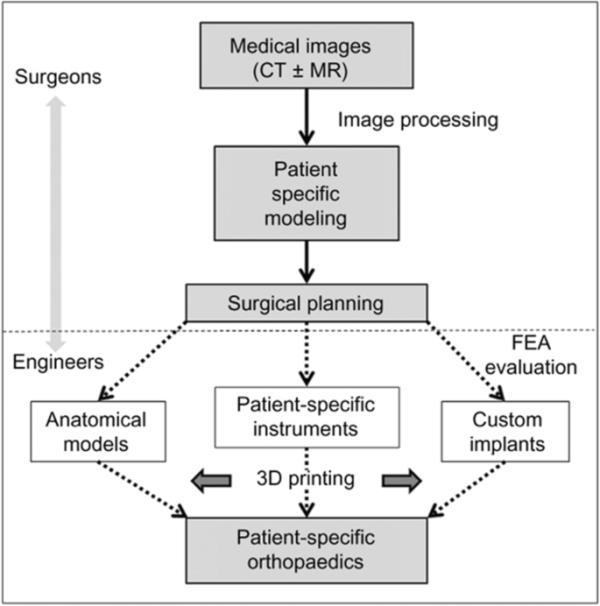
从图像采集的初始阶段开始,到3d打印模型和植入物的创建,涉及患者特定骨科模型和植入物生产的临床工作流程概述[23]
为了准确地描述不同受术者的解剖结构,必须精确地捕获骨结构。计算机断层扫描(CT)和磁共振成像(MRI)等医学成像方式通常用于获得高分辨率和精度的三维医学信息[24,25]。对于骨科应用,CT成像是首选,因为它具有高对比度和可靠的骨尺寸表现。然而,每次成像过程中受试者都需要麻醉,动物种类繁多,这是动物CT成像的两个主要缺点[24]。大多数CT机获取的医学图像以DICOM(医学数字成像和通信)格式导出,DICOM是一种用于传输、交换和存储医学图像的典型数据表示形式。因此,在骨科和3D打印程序中使用的接收器特定的健康成像记录通过DICOM插图连接起来。
图像处理阶段需要能够创建特定图像的软件(称为DICOM)来构建三维网格[24]。这是通过将dicom兼容文件中收集的数据传输到用于3D对象制造的商业或开源3D软件程序来实现的。这些程序采用MPR技术,利用薄轴向图像切片生成非轴向二维图像[23]。
在成像过程中需要额外的重建冠状图像来正确描绘复杂的3D结构,以改善临床可视化和解释。在检查肢体异常或骨折的骨骼结构和关节排列时,轴向元素的详细信息可能不太明显,这项技术非常有用[23]。另一种用于生成数据集的3D网格表示的3D模拟方法是体绘制。DICOM图像被转换成3D表示形式,然后可用于CAD文件创建或医疗诊断目的。CT重建方法、切片厚度、辐射强度等扫描仪因素对三维渲染结果的正确性有影响[23,26]。有几个商业软件包用于医疗应用,如ScanIP (Synopsys, CA, USA), Research Triangle Park, NC, USA), Geomagic Studio (Raindrop Geomagic), Mimics Innovation Suite (Materialise, Leuven, Belgium)。此外,还有Meshlab、Slicer和InVesalius等开源应用[24,27]。
分割图像:分区Ning可视化数据进行分析
3D打印的第一步包括分割DICOM表示以及创建stl模型。随后,导入DICOM文件,需要从图像数据中提取感兴趣的区域,通常是骨骼。分割是一种通过考虑图像数据中的特定密度和地形信息并去除任何不需要的或非解剖数据来隔离和提取感兴趣区域的技术。阈值分割是一种广泛使用的方法,用于将具有稳定强度差异的区域与其周围组织分离开来。分割后的孤立区域可用于构建三维模型[23,28]。将信息转换为3D-CAD合适格式的文件后,包括STL格式的中间信息,即可开始初级处理。三维模型质量与stl数据质量密切相关;因此,高质量的3D模型必须由高质量的STL数据创建。STL文件经过初始和后续处理,如孔校正和噪声消除后,可以用于3D打印。使用CAD软件,将结构的轮廓划分为不同的多边形,通常是三角形,以生成三维网格模型。3D模型的分辨率与使用的多边形数量直接相关,但这也会显著增加数据量和处理时间[23,28]。要将DICOM图片分割成STL数据,可以使用Mimics和3D Slicer等医疗软件。最终3D模型的正确性还可能取决于扫描因素,包括切片厚度、辐射强度和CT重建技术[23]。
数据的处理和检查
DICOM可以简单地导入到图像编辑包中,然后将其转换为STL标准3D格式。在将CAD数据发送到3D打印机以创建项目之前,不需要进一步修改STL文件,例如物体几何校正或三角网格优化,但这是可能的。如果有一些需要修改的形状或形式的对象,不管它是如何构建的,软件像Autodesk或免费软件,例如BRL-CAD (https:/brlcad.org/)或Openscad (https:/openscad.org/)可以利用[23,24,26]。
制作3D模型的关键步骤是创建STL数据,然后STL文件可以导入到与商业软件或打印机相关的专有应用程序中,例如带有Netfabb?和KISSlicer的Fusion 360或ReplicatorG。确保最后阶段包与正在使用的打印机兼容是至关重要的。为了打印实际的3D模型,利用“G-code”创建软件来创建G-code是很重要的。利用CAD程序将表示三维模型的STL文件划分为横截面层。3D打印方法可以通过依次添加材料层来创建3D物理模型。然而,该过程的每一步,包括STL分析、3D打印机输出、g代码数据创建和DICOM图像分割,都会影响最终3D模型的准确性[23,28]。
摘要
介绍
三维技术的进步
Nal印刷技术
我的应用
3D打印在生物医学中的应用
适合3D打印的材料
生物医学我
使用3D打印的tal制造
新兴趋势和重点领域
结论
数据和材料的可用性
参考文献
致谢
作者信息
道德声明
搜索
导航
#####
增材制造技术使得生产具有复杂内部结构的金属植入物和为特定个体定制的医疗植入物成为可能,这使得它们在临床环境中的应用非常有前景[29]。其中一个模型是使用3D打印来大量生产高度精确的解剖模型,骨科医生可以使用这些模型进行手术准备。此外,通过从患者的磁共振成像(MRI)或x射线计算机断层扫描(CT)图像创建计算机辅助设计(CAD)模型,3D打印技术可用于构建患者特定的植入物。因此,3D打印工艺是生产生物金属制成的医疗设备的理想选择。本节将介绍目前流行的3D打印生物金属的方法(图2)[30,31,32,33,34]。
图2
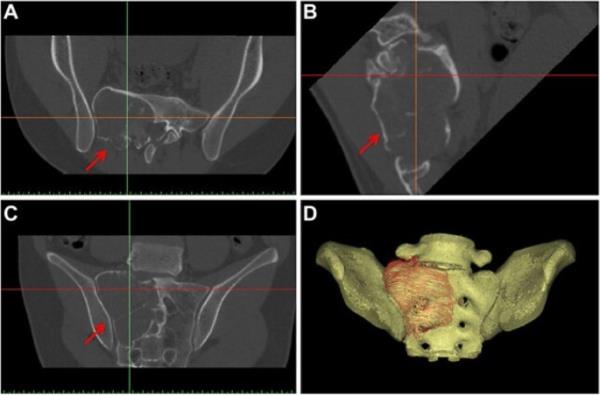
轴向计算机断层扫描(CT)图像从诊断为低级别骨肉瘤,影响骶骨的患者获得。感兴趣的区域由红色箭头表示[23]
SLS(选择性激光烧结)技术最早于1989年问世并获得专利[35]。液相烧结是在这一过程中使用的冶金机制。粉末致密化是通过液相凝固结合和固相颗粒重排来完成的。形成过程部分熔化粉末材料,同时保持其固相核心[36]。SLS的两个主要组成部分一般是粉末筒和成型筒。粉辊在粉筒中上升时,将物料粉均匀地分布在成型气缸的活塞上。计算机根据原型切片模型控制激光束的二维(2D)扫描路径,选择性地烧结固体粉末物质并生成一层样品。在每一层完成后,将功能活塞降低一层厚度,添加新的粉末,然后对新层进行激光扫描。直到层堆积创建所需的3D样本,这个过程是重复的。粉末不会完全熔化,因为SLS工艺中使用的半固态液相烧结机制阻止了它这样做。由于固相颗粒的存在,即使由成形材料的热引起的应力有所降低,所开发的组件也具有高水平的密度和孔隙率。这可能导致工艺缺陷,包括表面粗糙度差和抗拉强度低。尽管如此,SLS提供了一定的好处,包括广泛的成型选择和简单的成型程序(不需要任何支持)[37,38]。
SLM(选择性激光熔化)是一个自1995年以来一直存在的概念[36],其原理与选择性激光烧结(SLS)相同。SLM利用高能光纤激光器和精确的粉末扩散,使粉末完全熔化,实现金属部件的快速生产[39]。为了避免金属与SLM过程中高温下的其他气体相互作用,该腔室要么是惰性气体保护,要么是真空保护。利用更大的激光能量密度和更紧密的指向点,生产出具有优越尺寸精度和表面粗糙度的功能部件。SLM可以生产可操作的金属部件,而不需要中间操作。SLM制造的零件具有高密度、强机械性能和冶金粘合结构,无需后处理[40]。SLM不需要特别制备的原料,可以使用单一或多组分材料。SLM可以显著缩短生产时间,降低零件成本,同时提供设计自由度。SLM降低了材料浪费,可用于生产各种各样的材料。使用SLM可以直接生产具有复杂几何形状的功能部件,这使其成为生产单个或小批量部件的最佳选择。
近年来,选择性激光熔化(SLM)已成为快速成型研究的一个主要趋势[41]。SLM是一种多功能技术,能够打印各种材料,如聚合物[42]、金属[43]、金属-陶瓷混合物[36]和金属-聚合物混合物[44],从而能够制造几乎任何形状的近密度金属部件[39]。由于能够生产高精度、全冶金部件,SLM在医疗领域经常被用于制造具有优异生物相容性的复杂种植体[45]、股骨种植体[46]和牙科修复体[47]。医用金属,包括不锈钢、钛合金、镍基超级合金和钴基合金,通常使用SLM加工,因为它能够生产高精度和表面精加工的零件,而不需要传统工艺(例如机加工和铸造)可能需要的额外加工步骤[36]。SLM也非常适合制作具有精确比例的功能性或复杂梯度结构,这使得它非常适合制作金属支架和植入物[48]。因此,SLM 3D打印已经发展成为一种强大的增材制造方法,用于生产独特、复杂的生物金属设备[49]。
激光直接金属沉积(laser direct metal deposition, LDMD)自20世纪90年代被首次提出以来,在世界范围内得到了广泛的发展[50]。它也有不同的名称,如激光快速成形(LRF),激光工程净成形(LENS),定向金属沉积(DMD)等,但它们都有相同的基本原理。在LDMD中,激光束集中在一个点上,而喷嘴将金属粉末聚集在其操作平面上。激光照射的粉末在那里凝固,形成层状实体[51]。与SLS/SLM相比,LDMD使用喷嘴来分配金属粉末。它的优点是可以生产大量的零件,并在喷嘴中混合几种金属粉末以生产某些金属合金。LDMD可用于制造完整的零件,并用于添加、修复和涂覆特征结构。它有潜力生产具有孔或金属特定梯度的材料,如形状记忆合金、不锈钢和钛合金,它们比使用其他方法打印的材料在几何上更灵活[52]。如Xue等[53]采用LENS对承重骨进行了网状多孔钛[54]。与致密钛相比,多孔钛种植体的力学参数更接近天然骨,杨氏模量为2.6 ~ 44 GPa,机械强度为24 ~ 463 MPa。体外实验发现,理想孔尺寸大于200 μm时,细胞增殖和粘附增强。在长达16周的实验中,多孔Ti6Al4V合金样品中相互连接的孔隙显著提高了雄性Sprague-Dawley大鼠植入物内的钙含量,表明生物组织可能在植入物内发育。该研究还表明,种植体中孔的总数是组织长入的重要决定因素[55]。
由于激光聚焦光斑大,LDMD精度在1mm以上。可以生产出具有冶金结合的致密金属产品,但由于其尺寸精度和表面光洁度不理想,需要进一步加工才能使用。使用LDMD使用的层-添加剂技术,沉积材料在不同位置经历了几个复杂的热循环过程,包括熔化和在较低温度下的多次再加热循环。由于这种热行为引起的大量相变和微观结构变化,管理所需组件所需的结构和成分具有挑战性。尽管微小的激光束迅速形成熔池,但这会导致熔化不稳定并加速凝固。由于凝固过程中发生的快速温度变化所产生的复杂残余应力,ldmd形状的件可能会变形或断裂。LDMD技术的两个主要缺点是无法调节成分和微观结构以及残余应力的产生[56]。
3D打印技术利用高能激光源将金属材料(粉末、电线)熔化并融合成层,可以生产出具有与传统方法制造的机械性能相当的金属部件。然而,由于电子束或激光束的逐步扫描和堆积导致材料的快速加热和冷却产生了显著的温度梯度,并导致复杂残余应力的不均匀分散。这些残余应力会导致金属零件变形和开裂,并对其力学性能和耐腐蚀性产生负面影响[30]。有许多方法可用于减少或消除这些残余张力[57]:在设计阶段,(a)应仔细考虑最小化残余应力;(b)修改激光扫描方式,将扫描矢量旋转到下面的一个处理层,以防止类似路径上的压力集中;(c)应避免不间断烧结和大面积烧结;(d)在零件退火前应加热粉末床以消除应力。
SEBM使用高能电子束,通过加热和熔化精确图案的金属颗粒,快速制造3D样品。为了形成3D零件,首先在表面上涂上一层粉末,然后根据3D CAD文件信息对金属粉末进行选择性加热。磁导电子束帮助熔融粉末与下面的组件形成层层连接。然后除去多余的粉末以产生所需的3D样品[58]。扫描方式、加速电压、粉末厚度、作用时间、聚焦电流、电子束电流等过程变量的影响是目前研究的主题[59]。在SEBM中,金属粉末是用高能电子束熔化的,电子束由磁偏转线圈控制,不需要机械惯性。在熔化或烧结过程中,由于真空气氛,金属粉末不能氧化。与激光相比,电子束有几个优点,如维护成本高、稳定性好、操作成本低、材料吸收率高、能量利用率高。与其他技术相比,SEBM具有较小的零件变形,更高的效率,更密集的微观结构形成,并且不需要成型支撑。磁场用于调节电子束的聚焦和偏转长度,使电子束更快、更灵敏。这是通过调整电信号强度和方向来实现的。然而,由于电子束无法聚焦在一个小的位置上,因此很难实现高尺寸精度和复杂的成型物体设计[60]。
在具有外部多孔网状结构区域的生物金属装置中,如髋臼杯、髓内棒和股骨膝关节植入物,SEBM是一种常见的3D打印技术[61]。然而,由于SEBM的特性,如组件取向、光束流和粉末尺寸,为该方法在骨科植入物中的应用提供了困难,因此优化植入物的表面光洁度是一项挑战[62]。
由于与金属装置和粉末相关的高费用,打印过程可能相当昂贵,这可能相当于大量美元。随着制造业对金属3D打印的需求不断上升,更多的资源和科学研究正在投入到改进技术和提高成本效益上。正在开发的几种新方法在降低成本和鼓励制造新概念方面具有重大潜力,尽管它们尚未用于商业用途。
金属打印通常仅限于熔点较低的物质,这使得包括铜或金在内的金属的3D打印具有挑战性或昂贵。为了解决这个问题,最近创建了一种称为LIFT的技术[63]。LIFT是一种与传统金属3D打印工艺不同的直接打印技术,它使用了一种被称为“供体膜”的金属材料薄覆盖物。当脉冲激光将液滴对准供体薄膜时,液滴被喷射到被称为“接收器”的透明基板上,引起热压波或蒸发[64]。这项技术已经成功地应用于打印金属,如铬、金、钛、镍和铝[65,66]。然而,LIFT打印厚金属面临的挑战是在堆叠的液滴之间实现良好的粘附,导致低纵横比柱,球形形状,以及后续层之间的接触面减少。由于逐层沉积精度降低,很难产生大规模的三维结构和悬垂[67]。为了克服这些限制,可能需要牺牲支撑材料。LIFT已被用于制造生物传感器,最近的进展已经证明了用银/铜合金打印小型物体的能力[68]。报道的LIFT范围的横向尺寸在微米尺度上,最小尺寸接近3 μm[69]。在最近的测试中,铜和金被用作主要的构建块,以打印高2毫米,周长5 μm的3D塔。低能激光也被用来制造圆盘状液滴,这改善了层的堆叠[70]。
一种名为ADAM的新型3D打印方法最近被开发出来,用于逐层打印包裹在塑料粘合剂中的金属粉末[71]。印刷后,塑料粘合剂在烧结炉中分离,留下高密度(95-99%)的金属粉末。以前3D打印过程中出现的层间强度差的问题通过整个组件的同时烧结有效地解决了,这促使金属晶体通过粘合层形成。此外,ADAM打印机能够产生传统金属3D打印技术无法实现的几何比例。其最大印刷尺寸为250毫米× 220毫米× 200毫米。此外,它还提供基于云的在线过程激光检测,使客户能够密切关注每个打印层。打印机有一个远程云访问金属材料处理系统。该打印机可以3d打印303和17?4不锈钢,但是,它与A-2、Ti6Al4V和D-2钢的兼容性目前正在研究中。与传统的金属3D打印方法相比,ADAM的优点很多。它可以生成需要后处理的高质量零件表面,构建精确而复杂的结构,具有良好的各向同性性能,比传统加工快100倍,成本仅为传统金属3D打印的十分之一,最适合批量生产。
一种名为纳米颗粒喷射(NPJ)的新型金属3D打印技术于2016年发布。它与传统金属3D打印的不同之处在于,它不使用金属粉末颗粒,而是使用液体油墨将金属粉末颗粒包裹起来[72]。大的金属碎片被分解成纳米颗粒,并嵌入粘合剂中制造油墨,从而产生一致的油墨[72]。油墨的金属颗粒被分散和悬浮在油墨中,然后通过喷嘴排出,产生一层一层的打印。这种基于油墨的方法使整个产品平滑,这是有益的。打印过程使用标准喷墨打印头作为沉积工具。在印刷过程中,由于加热,室中任何多余的粘合剂都会蒸发,而金属组件将是所有剩下的。该工艺的精度约为1微米(m),成型温度约为300°C。由于每秒可以滴下2.21亿滴墨水,NPJ打印过程比标准激光打印快五倍。NPJ的使用节省了成本,减少了材料浪费,并且能够制造几乎任何复杂的形状。组件具有高水平的精度和表面质量,并且工作过程变得更容易和更安全。然而,与传统的金属3D打印相比,其耐温性较低,这仍然是其主要缺点。总的来说,NPJ是一种简单干净的方法,不需要设计和拆除复合支撑结构[71]。
在CAD文件的控制下,通过墨盒将精确的水射流分层打印到金属粉末床上[73]。所需的机械强度随后通过在炉中烧结打印的金属部件来实现。与其他3D金属打印工艺相比,这种方法无法使用激光或电子束来熔化金属颗粒。廉价的设备成本和热调节烧结过程是喷墨3d打印的关键优势。尽管喷墨3d打印的精度不如SLM、SEBM和LENS,但其快速、低成本制造生物金属器件的能力使其适合生物医学应用[74]。
基于挤压的3D打印由于其广泛接受,用户友好的性质,通过CAD精确打印复杂几何形状的能力以及各种凝固技术的利用,已经成为一种有前途的打印技术。然而,需要注意的是,这种方法需要使用具有特定印刷质量的材料[75,76]。与上述替代印刷方法相比,采用这种印刷方法相对更具成本效益,并且潜在的挑战性更小。此外,制造和几何参数可以很容易地调整,以满足用户的脚手架规格,如实现高模量和确保结构完整性等。这方面的一个例子是在逐层制造中使用圆柱形纤维,与其他3D打印方法(如液滴或喷墨制造)相比,它提供了增强的结构完整性。由于组织复制或结构支撑的复杂性,需要使用多种材料,导致需要多材料挤压[77,78]。多组分系统具有在各种生物结构中容易产生界面组织的能力,如器官发生、脉管系统、肌肉和骨骼。
使用基于挤压的3D打印,再加上随后的脱脂和烧结工艺,为多孔支架的生产提供了一种强大的方法。这种技术被证明特别有利的情况下,所涉及的材料构成重大困难时,受到替代增材制造方法。通过使用基于挤压的3D打印,有效地实现了具有铺设图案的多孔铁支架的制造。这些支架具有更好的生物可降解性,并表现出与天然骨非常相似的机械性能。因此,它们作为骨替代物具有很大的应用前景[78]。Putra等人采用基于挤压的3D打印方法制造可生物降解的Fe-Mg支架。这些支架具有非铁磁性,生物降解率提高[79]。这些支架有效地解决了生物可降解支架的主要限制,如生物可降解性低,与磁共振成像缺乏兼容性。Dong等人最近报道了一种基于挤压的增材制造方法,用于生产可生物降解的Mg-Zn/生物陶瓷复合支架。这些支架有望解决伴有严重节段性骨缺损的股骨骨不连[80]。生物陶瓷颗粒掺入镁基复合材料中,可调节镁基复合材料的生物降解动力学。与传统镁合金相比,镁基复合材料具有更好的细胞相容性和力学性能。
图3
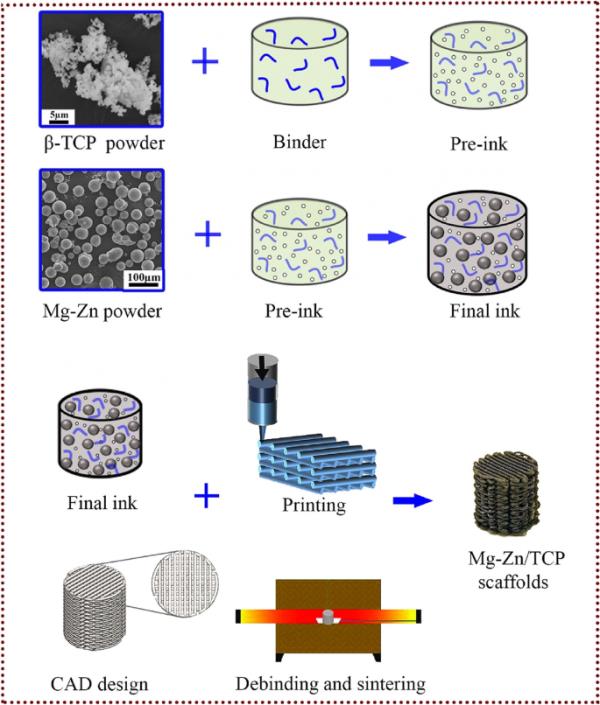
一个循序渐进的图表显示如何使用基于挤压的3D打印制造复合支架[80]
目前,许多研究正在进行中,以创造适合3D打印的新鲜生物材料[25]。术语“生物材料”是指有机或合成来源的化合物,这些化合物与来自生命的组织相结合,以维持、替代或再生器官或组织。用于3D打印的生物材料受到最终物体预期用途的影响[81]。例如,用于骨科3D打印的生物材料必须是可有效打印的,具有高生物相容性,可控制的生物降解,具有可用的机械性能,并具有设计有效的结构[81,82]。该物质在外科手术中必须是可消毒的[23]。尽管3D打印在许多医疗应用中都很有效,但现在只有少数材料可以用于3D打印。在骨科应用的3D打印中,最常用的生物相容性和可植入材料是超高分子量聚乙烯(UHMWPE)、聚醚醚酮(PEEK)、陶瓷、不锈钢(SS)合金、钴铬(CoCr)合金和钛(Ti6Al4V)合金[25]。3D打印中使用的生物材料根据其化学组成大致可分为四类[81]。
由于生物陶瓷具有可能的骨诱导和骨传导特性、高刚度以及与骨骼矿物相的相似性,生物陶瓷最近已被用于构建3d打印植入物[4,83]。羟基磷灰石(HA)是一种具有类似天然骨基质结构的人工材料,是磷酸钙陶瓷(CaP陶瓷)的组成部分。骨修复中常用的CaP陶瓷包括HA、TCP和BCP[84]。在植入后的前两周,生物活性玻璃,也被称为生物玻璃,是由合成硅酸盐组成的陶瓷,可以迅速被吸收,允许骨快速发育和植入物生长。尽管生物活性玻璃和CaP陶瓷被用于3d打印支架的生产,但这些材料的机械质量有限,例如断裂韧性差和拉伸强度差,使这些材料无法用于承载应用。尽管生物活性玻璃和为了克服这一缺点,生物陶瓷与聚合物如PCL、聚(D, l -乳酸-羟基乙酸)或纤维素结合,它们与碳纳米管、石墨烯、聚乙烯、Al2O3和TiO2等特殊增强材料混合,以生产具有更高机械强度的陶瓷复合材料[83]。由于其高生物相容性和成骨特性[85],石墨烯及其衍生物有可能在材料研究领域做出重大贡献。一个研究小组研究了体外填充犬脂肪来源间充质干细胞(cAD-MSCs)的石墨烯基支架的生物学和成骨特性。根据研究结果,碳可以增强cADMSC细胞的粘附、增殖和成骨分化,石墨烯基支架具有极强的生物相容性。在兽医学领域,已经提出了用于骨组织工程的新型材料,其中一种材料是基于石墨烯的支架[4]。陶瓷也被用于改善骨组织和植入物之间的骨整合,并限制植入物和骨之间发生的微运动。这是通过减少微运动的数量来实现的。陶瓷股骨头尚未用于兽医髋关节植入物的生产;尽管如此,通过类金刚石碳涂层的股骨头被用于生产最新一代的苏黎世无水泥髋关节[86]。
在3d打印骨骼替代品的生产中,聚合物的使用是一种常见的做法,因为它们有可能作为熔融沉积建模(FDM)的细丝、立体光刻设备(SLA)的解决方案、选择性激光烧结(SLS)的粉末珠和直接墨水书写(DIW)的凝胶[87]。这是因为聚合物可以用于这些能力中的任何一种。PDL、PLA、PGA或其共聚物以及PLGA是可用于3D打印过程的可生物降解聚合物[87]。3D打印经常使用PCL,它不仅是一种经fda批准的可生物降解聚合物,而且是一种可以自然分解的聚合物。由于其高水平的生物相容性、低降解率和令人满意的机械质量,PCL是生产3d打印骨支架的首选材料[5,88]。热塑性聚合物被称为高密度聚乙烯,简称HDPE,由于其具有良好的机械和热特性,在生物医学工程中得到了广泛的应用。聚乙烯被用作兽医全髋关节假体的承载面[88]。UHMWPE是兽医关节置换中使用最多的聚乙烯类型,也是最初使用的类型[86]。人类THR手术中使用的材料选择发生了重大变化[88],包括从HDPE转向UHMWPE。此外,接收器专用的手术指南、设备和假体可以由PLA和丙烯腈丁二烯苯乙烯(ABS)等热塑性聚合物制成。这些热塑性聚合物也可以用来制作肢体的3D模型。此外,聚酰胺以其稳定性、刚度、柔韧性和抗冲击性而闻名。最近的研究表明,聚酰胺和透明质酸偶联后可用于制造骨再生的多孔支架[89]。这些支架具有显著的承重能力,可用于制造多孔支架。
由于其出色的弹性、可调节的力学性能、生物可降解性和生物相容性,3d打印的水凝胶支架在目前的BTE定制支架制造中显示出巨大的潜力。水凝胶和生物墨水通常通过激光辅助生物打印、喷墨和挤出3D打印方法打印。由于其出色的弹性,可调节的力学,生物可降解性和生物相容性,3d打印水凝胶支架在为BTE量身定制支架方面显示出巨大的潜力。早期研究表明,挤压生物打印的细胞存活率可达98%[90]。动态结构水凝胶可以在分子水平上提高聚合物的愈合效率,从而最大限度地减少挤压打印过程中细胞的损伤。这种结构能够自我修复的程度,或者连续修复的次数,是定义其自我修复性能水平的两个特征。直接墨水书写,通常被称为DIW,被广泛认为是最常用于开发自我修复智能框架的技术[91]。
复合材料是一种通过结合两种或两种以上具有不同物理特性的元素来实现协同性能的人造材料。复合材料的多样化结构使其在保持适当的机械性能的同时具有高度的生物相容性,这使得它们在3D打印骨替代物中非常有用[83]。目前研究的复合材料包括PCL/PLGA/TCP、PLGA/TCP/HA和PCL/TCP。例如,PCL已与β - tcp结合,β - tcp是一种化合物,除了具有更好的骨导电性和可生物降解性外,还能够释放钙并促进骨形成。PCL/-TCP具有比PCL本身更强的诱导骨形成、刺激骨再生和替代骨的能力[92]。为了促进兔骨模型的成骨,采用不同比例n-HA的PLA/n-HA复合支架。结果表明,PLA/15% n-HA复合支架在兔模型缺陷中保留了其生物活性和合适的力学品质[93]。聚合物的低弹性模量使它看起来好像可以完全由它们制造假体装置;然而,它们的弱强度使得这种方法不合适。金属义肢不符合表面相容性标准并不罕见。正因为如此,大量的当代假肢由聚合物基复合材料制成,具有很高的强度重量比和高度的生物相容性[87]。
下载原文档:https://link.springer.com/content/pdf/10.1186/s13036-023-00371-7.pdf